세포 분열은 모든 살아 있는 유기체에 필수적인 과정입니다. 분열이 일어나기 전 매번 DNA에 저장된 세포의 유전 정보가 정확하게 복제되어야 합니다. 이 복제 프로세스는 DNA 복제로 알려져 있으며 적절한 조절을 통해 개체의 건강과 생존에 필수적인 역할을 수행합니다. 게놈 복제 시 높은 정확성을 달성하기 위해 세포가 DNA 복제를 조절하는 방식을 이해하는 것은 생물의학 연구에서 근본적인 질문 중 하나입니다. DNA 복제 중 발생한 오류는 인간의 건강을 위협하는 암과 같은 중증 질환과 관련된 게놈 불안정성을 유발할 수 있습니다. 실제로, 이전 연구에 따르면 모든 암의 최대 2/3가 DNA 복제 중 발생한 오류가 누적되어 유발되었다고 추정됩니다.
DNA 복제 분야의 개척자 소개
세포의 DNA 복제 방식은 Hana Polasek-Sedlackova 박사의 연구 분야이기도 합니다. Hana는 일찍이 중고등학교 재학 중 마사리크대학교(Masaryk University)에서 과학 연구 인턴십에 참여하여 실험실 및 DNA 연구를 접했습니다. 그 이후, 그녀는 이 분야에서 떠오르는 스타가 되었습니다. Hana가 쓴 학부 논문은 세계적으로 유명한 생명과학 학부상(Undergraduate Award in Life Sciences)을 수상했습니다. 이 상은 흔히 ‘주니어 노벨상’이라고 불립니다. 졸업 후 그녀는 노보 노르디스크재단(Novo Nordisk Foundation)으로부터 장학금을 받아 코펜하겐 생명과학 박사(Copenhagen Bioscience PhD) 프로그램에 참여했습니다. 이 장학금으로 Hana는 박사 과정 학생으로서 코펜하겐대학교(University of Copenhagen)의 노보노디스크재단 단백질 연구 센터(Novo Nordisk Foundation Center for Protein Research)에 소속된 Jiri Lukas 교수 연구실에 합류하여 박사후 과정을 이곳에서 계속했습니다. 그녀의 연구 논문은 Science 및 Nature와 같은 주요 과학 학술지에 게재되었습니다. 최근 그녀는 체코공화국 브르노에 있는 체코 과학원 생물물리학 연구소(Institute of Biophysics (IBP) of the Czech Academy of Sciences)에서 독립적으로 자신의 연구 팀을 시작했습니다.
과학 분야에 대한 그녀의 기여 중 하나는 MCM 역설을 푼 것이었습니다. 이 역설은 이 분야에 종사하는 과학자들 사이에서 1990년대부터 논쟁의 대상이었습니다. 현미경과 복제 중 발생하는 이벤트를 규명하는 데 사용된 다른 과학적 방법이 모순되는 것처럼 보이는 결과를 내놓았기 때문입니다. 이러한 모순은 이제 Hana가 애용하는 Evident의 scanR HCS(High-Content Screening) 스테이션 덕분에 성공적으로 해결되었습니다. Evident는 프라하의 분자유전학연구소(Institute of Molecular Genetics)에서 열린 scanR 사용자 모임에서 Hana를 만나 이 시스템을 사용해본 그녀의 경험과 이 시스템이 그녀의 연구에 미치는 영향에 대해 물어볼 수 있는 기회를 가졌습니다.
Evident와 Hana Polasek-Sedlackova의 인터뷰
Evident: IBP에서 자신의 연구 팀을 시작했을 때, 박사님께서 팀을 위해 가장 먼저 구입한 현미경은 scanR HCS(High-Content Screening) 스테이션이었습니다. 이 시스템을 선택한 이유는 무엇인가요??
Hana Polasek-Sedlackova: 연구 활동을 수행해 오면서 저는 여러 현미경을 사용해 볼 기회가 있었습니다. 이를 바탕으로 현미경을 선택할 때 고려해야 할 세 가지 중요한 조건이 있다는 것을 곧 깨달을 수 있었습니다. 그 세 가지 조건은 하드웨어, 소프트웨어, 고객 서비스입니다. 이러한 기준에서 저는 scanR이 최고의 HCS(High-Content Screening) 시스템이라고 생각했습니다.
첫째, scanR은 사용자의 구체적인 실험 요구 사항에 맞게 조정할 수 있는 간편하고 유연한 하드웨어 시스템을 갖추고 있습니다. 이 시스템은 광시야부터 초고해상도까지 다양한 이미징 기능과 고급 형광 현미경 기법 그리고 생세포 이미징 기능 등을 제공합니다.
둘째, scanR의 획득 및 분석 플랫폼은 직관적이고 사용자 친화적이므로 사용자는 짧은 시간 동안 고품질의 데이터를 다량으로 획득할 수 있습니다. 획득된 이미징 데이터를 활용하여 실시간 다변수 분석이 가능하므로 재스캔 기능과 같은 각종 유용한 기능을 통해 즉시 데이터를 검사하고 획득 매개변수를 더욱 최적화할 수 있습니다. (재스캔 기능은 관심 대상을 식별하기 위해 저해상도로 샘플을 간단하게 스캔한 다음 관심 대상을 고해상도로 다시 스캔할 수 있습니다.)
셋째, Evident는 탁월한 고객 서비스를 제공합니다. Evident의 현미경 유지 관리와 분석 지원을 담당하는 응용 전문가는 언제나 사용자의 요구 사항, 희망 사항 또는 문제와 관련된 도움을 줄 준비가 되어 있는 최고의 전문가들입니다. 우리는 체코과학재단(Czech Science Foundation)과 우리 연구소의 내부 기금 덕분에 scanR 기술을 구입하여 이 새 연구소에 도입할 수 있었습니다.
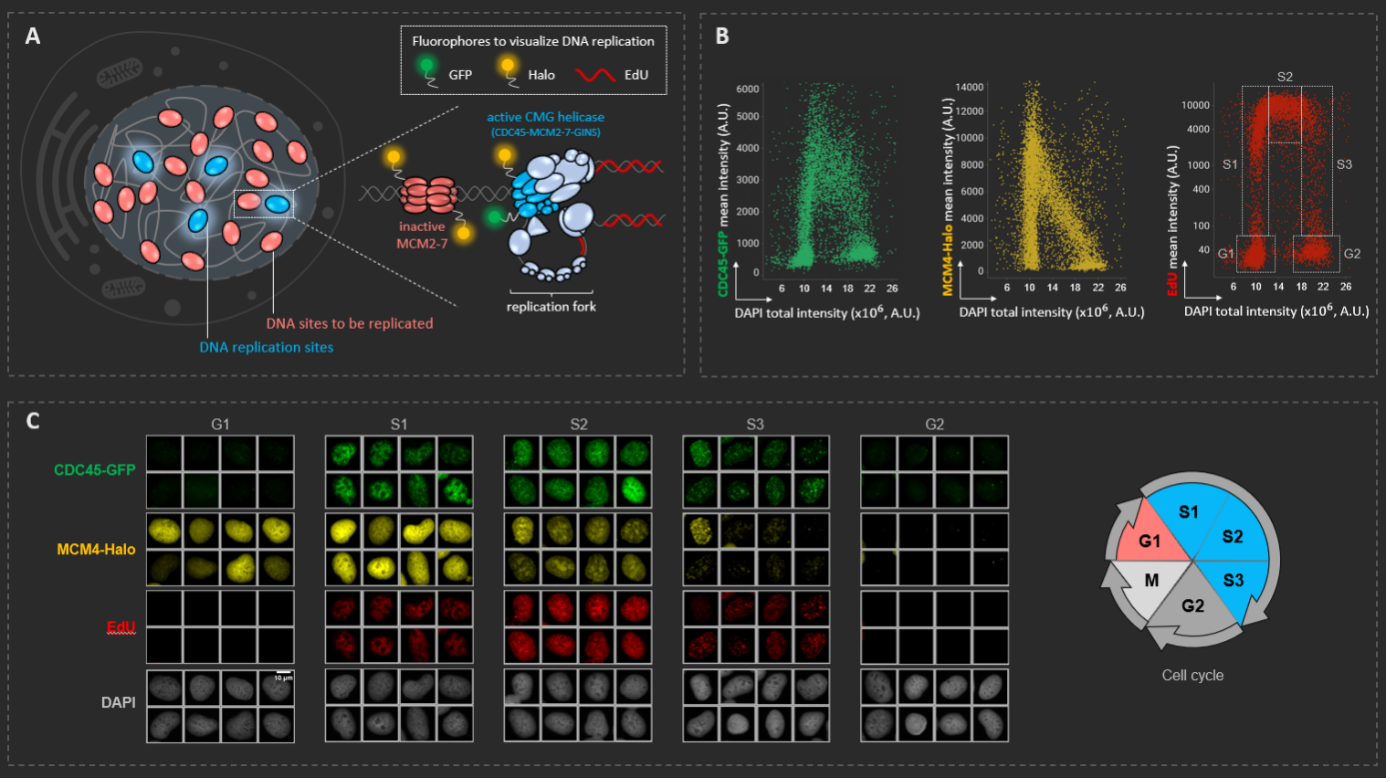
scanR 시스템으로 DNA 복제 역학 측정. (A) DNA 복제의 기본 단위인 단일 복제 분기점을 확대한 인간 세포 도식. 특이적 형광 프로브로 DNA에 대한 MCM 바인딩(Halo), 활성 CMG 나선효소 어셈블리(GFP) 및 DNA 합성(EdU)을 연구할 수 있습니다. (B) 인간 골육종 U2OS 세포의 DNA 복제 중 발생하는 주요 이벤트에 scanR 기반 다변수 분석에 적용. (C) 세포 주기 전반에서 DNA 복제 단백질의 역학을 보여주는 이미지 갤러리.
Evident: scanR 시스템이 박사님의 연구에 어떤 진전을 가져다 주었나요? scanR 시스템의 도움으로 새로운 발견을 하게 된 예를 들어주시겠어요?
Hana: scanR 시스템의 도움으로 우리는 DNA 복제 분야에서 중대한 발견을 할 수 있었습니다. 이 시스템은 MCM2-7 단백질 복합체의 행동과 관련된 오랫동안 풀 수 없었던 퍼즐인 MCM 역설을 푸는 데 중요한 역할을 했습니다. MCM 복합체는 복제 나선효소의 핵심부를 형성하며, 이 핵심부는 정확한 복제를 위해 이중 나선 DNA를 푸는 일을 담당합니다. 수년 동안 연구자들은 널리 보고된 역설적 사실 두 가지 때문에 당혹했습니다. (1) 5~10%만이 활성 복제 나선효소로 사용된다면 세포는 왜 비활성 MCM을 과도하게 많이 갖고 있는가? (2) 진핵 MCM은 현미경 접근법을 통해 세포 내부의 복제 부위에서 왜 시각화된 적이 없는가?
우리는 최근 계속되어온 개념적 교착 상태를 다시 들여다보고 MCM 역설에 대해 명쾌한 해답을 내릴 수 있었습니다. CRISPR-Cas9 게놈 편집과 scanR 고함량 이미징을 사용하여 살아 있는 세포의 DNA 복제 분기점을 이미징함으로써 오랫동안 계속된 문제를 규명하고, 게놈의 무결성을 보호하는 데 필요한 DNA 복제 출발점의 새로운 항상성 경로를 밝혀냈습니다.1-2
우리는 과도한 양의 비활성 MCM이 DNA 복제 중 발생하는 오류를 최소화하기 위해 복제 분기점 속도를 조정하면서 자연 복제 중단 부위(natural replication pausing site, NRPS) 역할을 수행한다는 것을 알게 되었습니다. 이러한 특성 때문에 NRPS는 암 세포가 자주 악용하는 또 다른 층의 복제 분기 속도 제어 장치를 대표한다고 할 수 있습니다. 따라서 NRPS는 암치료를 위한 매력적인 새 표적이 됩니다. 현재 저의 연구 팀은 DNA 복제 출발점에서 가장 정점에 있는 조절 경로와 이러한 경로가 인간 조직 발달의 병태 생리적 상태에 기여하는 바를 연구하고 있습니다.

scanR을 사용하여 MCM 복합체 단백질 종을 탐구함으로써 MCM 역설을 조명할 수 있었습니다. (A) MCM 단백질 풀을 구분하기 위한 HaloTag 라벨링 프로토콜. scanR 기반 고함량 분석을 통해 DNA 복제 프로그램 도중 모체와 초기 MCM 단백질 복합체의 다양한 역학을 밝힐 수 있었습니다. (B) DNA 복제 중 모체와 초기 MCM이 뚜렷하게 수행하는 기능을 설명하는 모델. 모체 MCM은 주로 활성 CMG 나사효소로 전환되지만, 초기 MCM은 대부분 비활성 상태로 남아 복제 분기점의 적절한 움직임을 지원하는 데 중요한 자연 리플리솜 중단 부위로서 기능합니다.
Evident: scanR 시스템을 사용하는 응용 분야와 이미징하는 샘플의 종류는 무엇인가요?
Hana: 우리는 연구를 위해 대부분 인체 샘플에서 유래한 다양한 조직 배양 모델을 사용합니다. 그 예로는 뼈, 유방, 난소, 자궁경부 또는 신장과 같은 다양한 조직에서 얻은 암세포주와 이들의 비암성 요소, 줄기세포 및 섬유아세포를 들 수 있습니다. 가끔은 연구에 동물 샘플도 활용합니다. 우리는 다양한 세포 생물학, 생물의학 및 유전학 접근법을 샘플에 적용하여 오류 없는 게놈 복제에서 중요한 역할을 수행하는 새로운 단백질이나 전체 조절 경로를 찾습니다. 또한, 암세포에서 이러한 새로운 단백질 또는 경로가 어떻게 조절되는지, 그리고 이것이 종양 발생에 영향을 주는지 연구합니다. 영향을 주는 것으로 나타날 경우 이러한 지식을 활용하여 암치료를 위한 새로운 접근법을 개발할 수 있습니다.
DNA 복제에서 새로운 단백질 요소를 찾아내기 위해 일반적으로 우리가 의존하는 실험 파이프라인은 대규모 단일 세포 모집단을 프로파일링하는 것입니다. scanR 시스템은 이와 관련하여 엄청 큰 도움을 주었습니다. 예를 들어, 새로운 단백질 후보를 찾은 경우, 다양한 방법을 사용하여 세포에서 해당 물질을 먼저 하향 조절합니다. 그 다음, 고함량 이미징을 통해 단계적으로 DNA 복제 정확성을 모니터링합니다. 실험에 세포를 사용하면 얻을 수 있는 장점은 자연적인 환경에서 게놈 복제 과정을 관찰할 수 있다는 것입니다. 그러나 그 복잡성 때문에 데이터 해석이 어려워질 수 있습니다.
따라서, DNA 복제를 연구하면서 관심 대상 유전자의 고갈이 세포 주기, DNA 손상 반응, 전사, 염색질 유지관리, 특정 염색체 영역의 유지관리, 전체 게놈의 안정성 등 다른 세포 과정에 어떻게 영향을 미치는지 주의해서 관찰해야 합니다. scanR 시스템은 매우 짧은 시간 동안 대규모 단일 세포 모집단에서 이처럼 편향되지 않은 정량적 프로파일을 얻을 수 있기 때문에 데이터를 신속하게 해석하고 연구를 효율적으로 진전시키는 데 큰 도움이 됩니다.
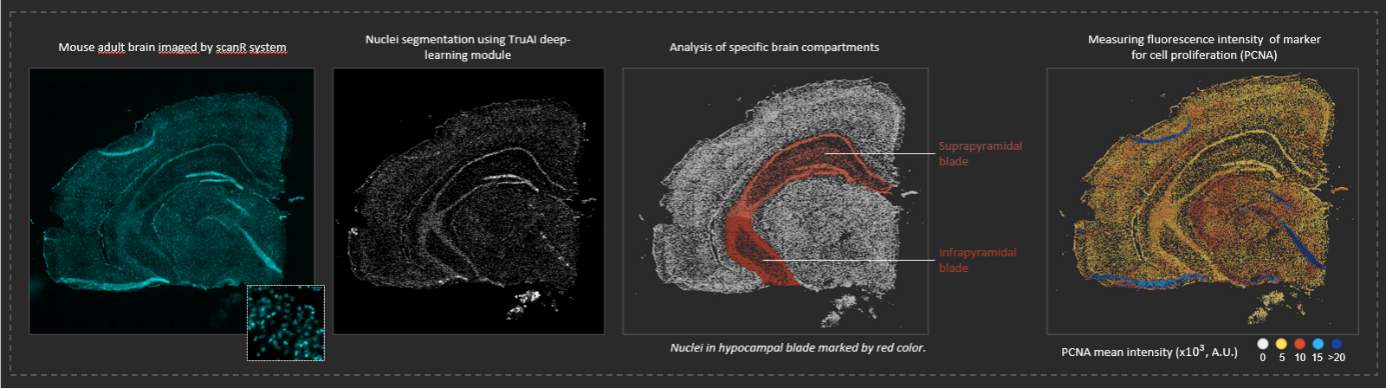
TruAI 딥러닝 모듈을 사용한 생쥐 성체 뇌의 개별 세포에 대한 이미지 분석. 뇌 샘플은 Jana Krejci 박사가 제공했습니다(생물물리학 연구소 세포 생물학 후생유전학부(Department of Cell Biology Epigenetics at the Institute of Biophysics)).
저는 현미경으로 수동 이미지를 획득하며 몇 시간씩 보내곤 했습니다. 그 후에는 이미지를 컴퓨터로 분석하는 데 훨씬 더 많은 시간을 쏟았습니다. 이 실험을 마치는 데는 수개월이 걸리곤 했습니다. 이제 scanR이 있으니 단 몇 시간 안에 모든 작업을 완료할 수 있습니다.
Evident: 이러한 응용 분야에 scanR시스템의 고함량 분석 기능과 이미지 기반 세포측정 접근법을 어떻게 활용하고 있나요?
Hana: 저는 세포 생물학에서 편향되지 않은 정량적 정보를 이미지와 결합하는 것이 필수 세포 프로세스를 보여주는 신뢰할 수 있고 정확한 방법이라고 생각합니다. scanR 시스템은 이를 위한 적절하고 스마트한 해결책을 제공합니다. 앞서 언급했듯이, scanR 시스템은 완전 자동화된 샘플 획득과 분석을 지원하므로 세포 프로세스에 대한 편향되지 않은 정량적 정보를 얻을 수 있습니다. 또한 중요한 장점은 클릭 한 번으로 데이터를 뒷받침하는 이미지를 직접 검사할 수 있다는 것입니다.
이와 더불어, 세포의 수명 내내 관심 단백질의 역학을 보여주는 편향되지 않은 이미지 갤러리를 만들 수 있습니다. 이러한 고유한 이미지-데이터 결합 덕분에 핵 또는 세포질과 같은 특정 격실 및 DNA 수리 병소 등의 부핵 격실에 대한 세포 프로세스 분석을 추가로 미세 조정할 수 있습니다. 이처럼 정량적 데이터를 시각적으로 보완하면 생물학적 문제를 더 효과적으로 해결하는 데 도움이 됩니다.
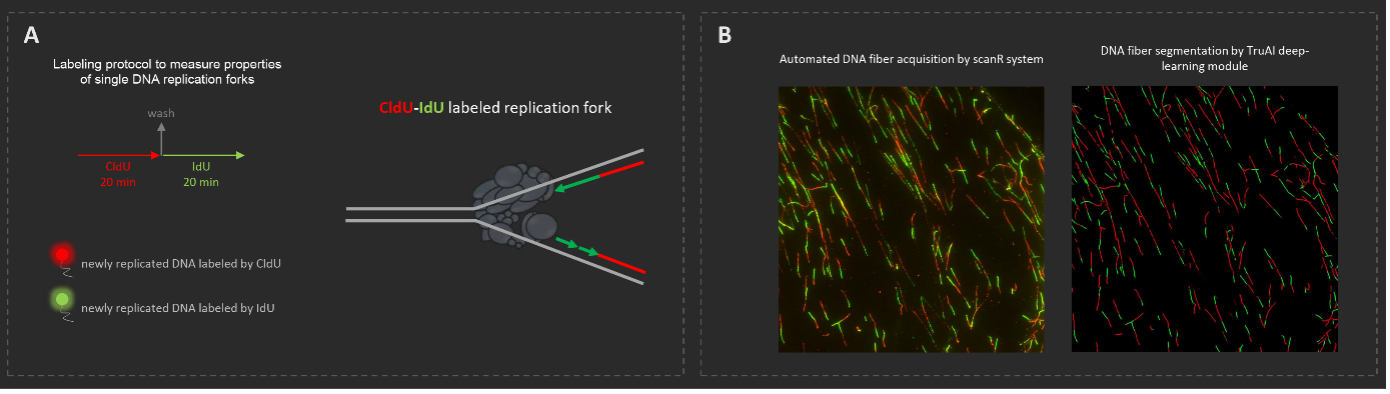
scanR과 cellSens™ 시스템을 함께 사용하여 진행되는 DNA 섬유 자동 획득 및 분석 작업의 예. (A) 단일 복제 분기점 시각화를 위한 CldU-IdU 라벨링 프로토콜. (B) scanR 시스템 및 cellSens™ 소프트웨어를 사용한 자동 DNA 섬유 획득 및 분할의 예.
Evident: 이 시스템 때문에 세포 생물학 및 분자 생물학을 위한 도구로서 현미경을 바라보는 방식이 바뀌었나요? 그리고 시스템이 제공하는 TruAI™ 딥러닝 기능을 사용하시나요?
Hana: Jiri Lukas의 실험실에서 박사 과정을 밟는 동안 고함량 이미징 및 scanR 시스템을 접했습니다. 이 혁명적 기술은 세포 생물학과 연구 전반에 대한 제 관점을 완전히 바꾸어 놓았습니다. 저는 편향되지 않은 완전 자동화된 세포 프로세스 분석 기능 때문에 특히 깊은 인상을 받았습니다. 과학 연구에서 현존하는 재현성 위기를 볼 때, 저는 연구자들이 완전 자동화된 방식으로 데이터를 획득하고 분석하도록 지원하여 세포 프로세스를 편향되지 않은 방식으로 표현하는 도구를 활용해야 한다고 확신합니다.
지금과 같은 인공지능(AI)의 시대에 이미지 분석은 이전의 한계를 초월했습니다. scanR 시스템은 이제 TruAI 딥러닝 모듈을 제공합니다. 이 모듈은 제 연구의 범위를 확장했습니다. 이전에 저는 주로 대량으로 배양된 인간 세포주에서 단일 세포를 분석하는 데 중점을 두었습니다. 그러나, AI 모듈을 사용하면, 예를 들어, 조직 절편에서 개별 세포에 대한 매우 정밀한 이미지 분석을 수행할 수 있습니다.
이미지 분석 역량의 한계를 넓힐 수 있는 방법의 또 다른 예는 scanR 및 cellSens™ 시스템을 함께 사용하는 것입니다. 이렇게 하면 DNA 섬유 기법으로 준비된 DNA 복제 분기점과 같이 단일 모듈에 대한 완전 자동화된 획득 및 분석을 수행할 수 있습니다. 이와 같은 예는 제 실험실에서 현재 진행 중인 새로운 응용 분야들 몇 가지를 보여줍니다. 우리는 다른 연구자들도 곧 이러한 도구를 활용하여 세포 생물학 분야에서 위대한 발견을 할 수 있기를 바랍니다.
Evident: scanR 시스템에서 가장 마음에 드는 점은 무엇입니까? 연구자들의 반응은 어땠습니까?
Hana: 저는 scanR 시스템의 다양한 기능들이 마음에 듭니다만 하나만 꼽자면 “자동화된 획득 및 분석 간의 고유한 연결”입니다. 이러한 연결 덕분에 우리는 획득된 이미지에 대해 실시간으로 다변수 분석을 수행할 수 있습니다. 저는 박사 과정 학생이었을 때 이 기능에서 깊은 인상을 받았습니다. 우리 연구소의 소규모 scanR 사용자 커뮤니티의 모든 새로운 사용자도 저와 똑같이 깊은 인상을 받았습니다.
제 동료 중 한 명이 이 경험을 다음과 같이 잘 요약했습니다. “저는 현미경으로 수동 이미지를 획득하며 몇 시간씩 보내곤 했습니다. 그 후에는 이미지를 컴퓨터로 분석하는 데 훨씬 더 많은 시간을 쏟았습니다. 이 실험을 마치는 데는 수개월이 걸리곤 했습니다. 이제 scanR이 있으니 단 몇 시간 안에 모든 작업을 완료할 수 있습니다.”
scanR 시스템에 대한 자세한 정보
scanR HCS(High-Content Screening) 스테이션을 사용한 경험을 공유해 주신 Hana Polasek-Sedlackova 박사님께 감사의 인사를 드립니다. scanR 시스템과 Evident의 다른 생명 과학 연구 솔루션에 대한 자세한 내용은 Evident에 직접 문의하거나 현지 Evident 영업 담당자에게 문의하세요.
Hana Polasek-Sedlackova 박사 사진, 제공자: Jana Mensatorova.
참고 문헌
- Polasek-Sedlackova H, Miller TCR, Krejci J, Rask MB, Lukas J. Solving the MCM paradox by visualizing the scaffold of CMG helicase at active replisomes. Nat Commun. 2022 Oct 14;13(1):6090. doi: 10.1038/s41467-022-33887-5. PMID: 36241664; PMCID: PMC9568601. https://www.nature.com/articles/s41467-022-33887-5
- Sedlackova, H., Rask, M.-B., Gupta, R., Choudhary, C., Somyajit, K., Lukas, J. (2020, October 21). Equilibrium between nascent and parental MCM proteins protects replicating genomes. Nature News. https://www.nature.com/articles/s41586-020-2842-3

