Im Gespräch mit Dr. Peter Ertl, Professor und Leiter des Zellchip-Forschungsteams an der Technischen Universität Wien (TU Wien) in Österreich, erfuhr ich einige faszinierende Fakten über seine Arbeit mit Lab-on-a-Chip-Technologien. Diese winzigen, autarken Systeme können für unterschiedliche Untersuchungen eingesetzt werden – von der Toxizität von Krebsmedikamenten bis zur Durchlässigkeit der Blut-Hirn-Schranke. Aktuell wird mit dieser Technologie ein COVID-19-Diagnosetest entwickelt, der innerhalb weniger Minuten genaue Ergebnisse liefern könnte.
Für Dr. Ertl fehlt den derzeitigen COVID-19-Diagnosemethoden die Kombination aus Schnelligkeit, Empfindlichkeit und Zuverlässigkeit, die für eine angemessene Bekämpfung der aktuellen Pandemie erforderlich ist. „Einerseits kann ein PCR-Test alles nachweisen, aber er ist nicht skalierbar und es dauert in der Regel bis zu 24 Stunden, bis ein Ergebnis vorliegt. Das Ergebnis ist nur ein paar Tage lang gültig, d. h. Sie können nicht an langfristig geplanten Veranstaltungen, wie Konferenzen, teilnehmen. Die derzeitigen alternativen Methoden wie Lateral Flow und Antigentests sind einfach nicht empfindlich genug. Sie können zwar bei symptomatischen Personen mit hoher Viruslast gute Ergebnisse liefern, aber ebenso wichtig ist es, asymptomatische Personen zu erkennen, die die Krankheit unbemerkt weiterverbreiten.”
Entwicklung eines wirksamen, effizienten COVID-19-Diagnoseinstruments unter Verwendung von Biochips mit Datenübertragungsfunktion
Zur Behebung dieser Schwachstellen entwickelten Dr. Ertl und sein Team eine Biochip-Technologie, mit der sich bereits 3 bis 5 Viruspartikel innerhalb weniger Minuten zuverlässig nachweisen und falsch-negative Ergebnisse ausschließen lassen. Auf diese Weise können auch asymptomatische Personen definitiv diagnostiziert werden, sodass sie sich selbst isolieren können, um die Verbreitung von COVID-19 einzudämmen.
Der Biochip ist so konzipiert, dass er über eine eigene Stromversorgung, eine Anzeigeeinheit und die Fähigkeit zur drahtlosen Datenübertragung verfügt (Abbildung 1). Die Ergebnisse können direkt und unverzüglich an das jeweilige epidemiologische Zentrum weitergeleitet werden. Diese Rationalisierung der Datenerfassung könnte erheblich dazu beitragen, genaue Fallzahlen und Ausbrüche zu melden.
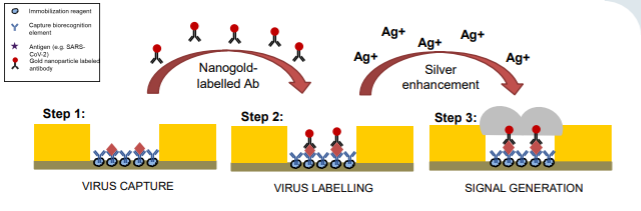
Abbildung 1: Funktionsweise des COVID-19-Biochips Bei der Biochip-Technologie wird ein Antikörperrasen genutzt, der auf der Mikrofluidikkammer immobilisiert ist. Dieser bindet jedes in der Probe vorhandene Zielvirus, in diesem Fall das SARS-CoV-2-Virus, das COVID-19 verursacht. Anschließend bindet ein sekundärer, mit Nanogold markierter Antikörper an die gebundenen viralen Partikel. Durch Zugabe einer Silberlösung in dieser Phase reagiert das Silber mit dem Gold und es entstehen leitfähige Nanobrücken. Dadurch kann ein elektrischer Strom fließen, LEDs aktivieren oder sogar eine Verbindung zu einem integrierten Kommunikationsgerät herstellen, um die Daten drahtlos zu übertragen.
Rolle der IXplore Live Cell Imaging Plattform von Olympus bei der Validierung des COVID-19 Biochip-Tests
Die ordnungsgemäße Funktion der Technologie hängt von der Qualität der Antikörper und deren Immobilisierung auf der Oberfläche der Mikrofluidikkammer sowie dem Abstand zwischen den unterbrochenen elektrischen Leitungen ab. Um diese zu optimieren, testeten Dr. Ertl und das Zellchip-Forschungsteam verschiedene Immobilisierungsstrategien. Mit dem Mikroskopsystem IXplore Live von Olympus und sekundären, fluoreszenzmarkierten Antikörpern konnten sie die für den Erfolg des Biochips entscheidenden Parameter wie Antikörperdichte, Orientierung und Ausrichtung bewerten (siehe Abbildung 2).
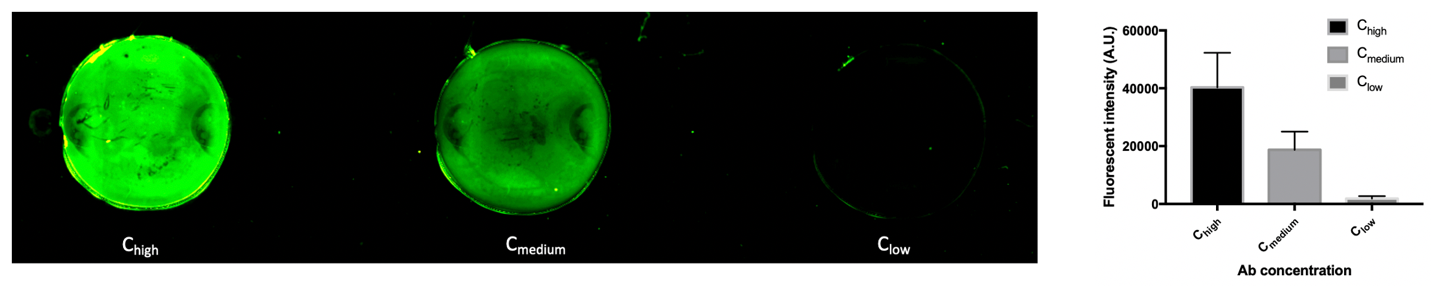
Abbildung 2: Verwendung des IXplore Live Mikroskops von Olympus sowie sekundärer fluoreszenzmarkierter Antikörper zur Bestimmung der Dichte immobilisierter Ziege-Anti-Ratte-IgG-Antikörper auf einem Glasträger bei 4-facher Vergrößerung. Das Bild zeigt abnehmende Antikörperkonzentrationen (von links nach rechts) entsprechend der abnehmenden Fluoreszenzintensität.
Dr. Ertl dazu: „Das Bildgebungssystem IXplore Live erwies sich für die Chipentwicklung als hilfreiche und kosteneffektive Lösung, die genau die erforderliche Bildauflösung bietet. Unabhängig von COVID-19 ist es zum beliebtesten System unseres Labors geworden und wird ständig für unsere Organ-on-a-Chip-Projekte eingesetzt. Insbesondere die hervorragende Auflösung, die Hypoxiekammer und die Möglichkeit, das System für konfokale Bildgebung aufzurüsten, waren für unsere Forschung von großem Nutzen.”
Anwendungen für andere Krankheiten, beispielsweise Krebs und Morbus Parkinson
Die Biochip-Technologie wird nicht nur für die Virusdiagnostikplattform, sondern auch für eine Vielzahl weiterer interessanter Anwendungen genutzt. Im Labor von Dr. Ertls wird an modernen Mikrofluidik-Zellkultursystemen geforscht, an so genannten Organ- oder Tissue-on-a-Chip-Sytemen, die die komplexe 3D-Architektur von Geweben und Organen nachbilden können. Diese Biochips werden nicht nur als biologische Modelle zur Untersuchung der Struktur und Funktion von Geweben verwendet, sondern geben auch Aufschluss über die Entstehung und den Verlauf von Krankheiten wie Krebs, Autoimmunerkrankungen und neurodegenerativen Erkrankungen.
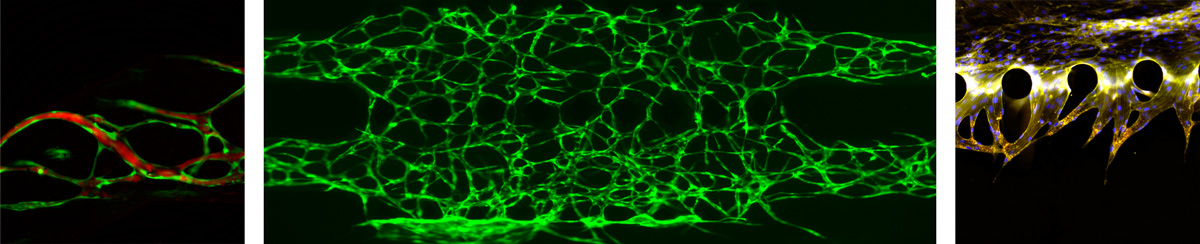
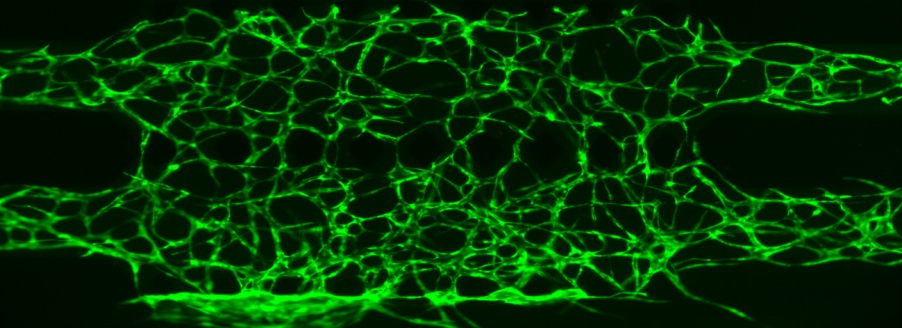
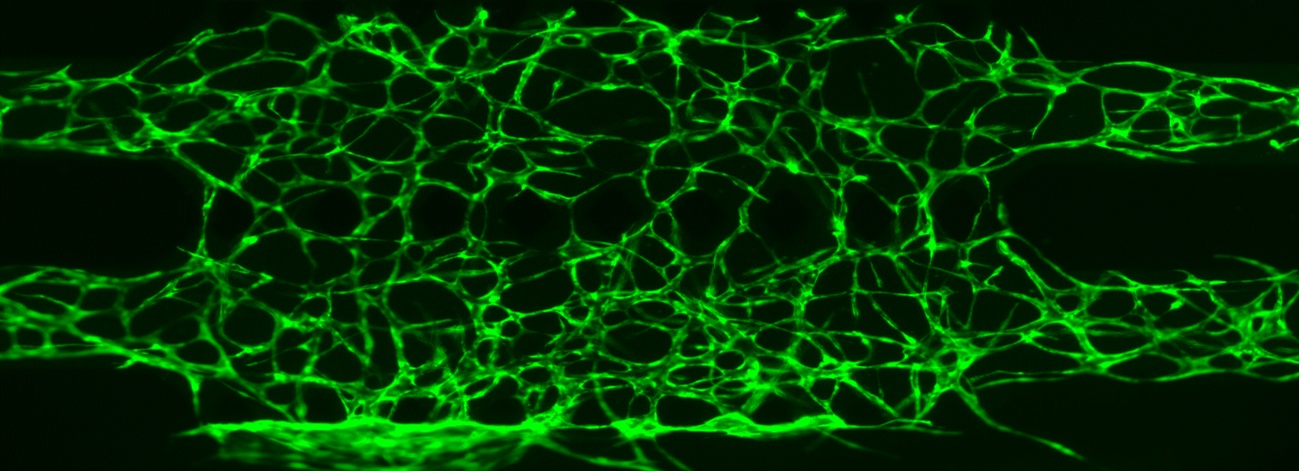
Abbildung 3: Die Bilder wurden vom Forschungsteam der TU Wien mit dem IXplore Live Mikroskop von Olympus aufgenommen. Von links nach rechts zeigen die Bilder (1) GFP-markierte HUVECs mit TRITC-Dextran-Perfusion (20-fache Vergrößerung) (2) GFP-markierte HUVECs (4-fache Vergrößerung) (3) DAPI-markiertes F-Actin und VE-Cadherin (20-fache Vergrößerung).
Dr. Ertl erklärte, dass das IXplore Live Mikroskop ein wichtiges Werkzeug für die Organ-on-a-Chip Forschung geworden sei. Die hohe Auflösung ist für die Validierung des 3D-Zellaufbaus unerlässlich, um sicherzustellen, dass die Architektur der tatsächlichen menschlichen Gewebestruktur nachempfunden ist. So hat das Team an der TU Wien das IXplore Live Mikroskop zur Beobachtung der Entwicklung der Lymphe-Blut-Schranke sowie für die Entwicklung einer sensorintegrierten Parkinson-Plattform auf einem Chip eingesetzt. Im letztgenannten Projekt war das Mikroskop IXplore Live von zentraler Bedeutung für die Untersuchung des Neuritenauswuchses und der Kalziumdarstellung. Das Forschungsteam hofft, dass daraus ein personalisiertes menschliches Mittelhirnmodell hervorgehen wird, das unser Verständnis der Aspekte von Morbus Parkinson im Zusammenhang mit der neurologischen Entwicklung verbessern wird.
Darüber hinaus stellte die Gruppe fest, dass die Möglichkeit, das IXplore Live Mikroskop mit einer Hypoxiekammer zu kombinieren, für die Entwicklung fast aller Mikrofluidiksysteme von großer Bedeutung war. Sarah Spitz aus der Forschungsgruppe von Dr. Ertls dazu: „Wir untersuchen mit der Hypoxiekammer hauptsächlich die Sauerstoffdurchlässigkeit verschiedener Materialien zur Herstellung von Mikrofluidikgeräten. Die Sauerstoffdurchlässigkeit ist ein wichtiger Parameter, da sie die Verfügbarkeit von Sauerstoff für die gezüchteten Zellen beeinflusst. Mit diesem Aufbau und einem im Chip integrierten Sauerstoffsensor können wir diese charakteristischen Eigenschaften sehr einfach bestimmen.”
Potenzial der Biochip-Technologie über COVID-19 hinaus
Virustests auf Biochips sind nicht nur ein potenziell schnelles und zuverlässiges Mittel zur Überwachung der aktuellen Pandemie. Investitionen in die Plattform könnten sich auch für die Diagnose anderer Krankheiten als nützlich erweisen. Da sich der Biochip selbst mit Strom versorgt und tragbar ist, könnte er in abgelegenen Gebieten oder an Orten eingesetzt werden, wo die Lagerung von Impfstoffen ein Problem darstellt, z. B. für Hepatitis B in Pakistan und Ebola in Afrika. Auch die Zukunft der Organ-on-a-Chip-Technologie ist vielversprechend und lässt spannende Entwicklungen bei der Behandlung vieler Krankheiten erwarten. Professor Ertl geht davon aus, in den nächsten Monaten den ersten industriellen Prototyp für den COVID-19-Test entwickeln zu können.
Ähnliche Artikel
Leitfaden für Remote-Mikroskopie: 6 Tipps für den Erfolg im Labor